
基因工程猪模型揭示免疫细胞“致命对话”
亨廷顿病(HD)又称大舞蹈病或亨廷顿舞蹈症,是一种由HTT基因CAG重复序列异常扩增引起的常染色体显性遗传性神经退行性疾病。该病的核心病理特征极为明确:纹状体中的中型棘状神经元发生选择性死亡。然而,驱动这种选择性神经元丢失的精确机制,尤其是神经免疫系统在其中扮演的角色,长期以来一直是领域内亟待破解的谜题。
2月24日,一项发表于《自然-生物医学工程》的研究为这一谜题提供了突破性的答案。来自暨南大学研究员闫森、教授李晓江团队,利用其自主研发的HD基因工程猪模型(HD-KI猪),结合单核转录组学、空间转录组学及T细胞受体测序等高精度技术,首次证实了T细胞浸润与HD选择性神经退行性变之间存在直接因果关系,系统揭示了一条从固有免疫启动到适应性免疫执行的完整免疫病理通路。

相关研究发表于《自然-生物医学工程》截图。研究团队供图,下同
《自然-生物医学工程》审稿人给予这项研究高度评价:“该研究利用前期已建立的HD-KI猪模型,该模型相较于其他物种(如小鼠)更能真实再现人类HD中纹状体神经元变性的过程,为深入探究导致选择性神经退行的潜在机制提供了独特平台。研究充分展现了HD-KI猪模型的价值,为理解人类HD病理中特定神经元的易感性提供了关键见解。”
大动物模型破解传统局限
长期以来,神经炎症被认为是HD病程的重要参与者。小胶质细胞的激活、炎症因子的上调在患者和动物模型中均有观察到。然而,适应性免疫细胞,特别是T细胞,是否能够进入大脑实质,以及它们是否直接参与了神经元的损伤过程,始终缺乏直接证据,成为领域内悬而未决的争议焦点。
论文共同第一作者、暨南大学附属广州红十字会医院博士后李嘉威指出,造成这一认知瓶颈的核心原因之一在于模型系统的局限。传统的HD小鼠模型(如转基因小鼠或敲入小鼠)虽然能够模拟部分分子病理特征,如突变亨廷顿蛋白的聚集,但它们无法再现人类患者最核心的病理变化——纹状体神经元的大规模、选择性丢失。没有神经元死亡,也就难以观察与之可能相关的免疫事件。
面对这一瓶颈,闫森/李晓江团队自2021年起历时5年攻关。他们大胆假设:T细胞浸润可能是人类及大动物模型特有的病理事件。论文共同通讯作者闫森对《球探体育比分:科学报》表示,研究的最大困难在于,长期以来依赖的小鼠模型并未发现T细胞浸润现象,这容易让人忽视T细胞在HD中的潜在作用。团队需要克服传统思维,结合对HD患者和HD-KI猪的数据进行大胆假设,并通过多维度实验小心求证。
“我们利用能真实模拟人类HD选择性神经退行病理的HD-KI猪模型,首次绘制了HD纹状体的跨物种单细胞图谱,并首次证明了T细胞浸润与HD病理之间的直接关系。”闫森表示,这一突破为HD的发病机制提供了全新视角。
细胞图谱揭示“致命对话”
在国家重点研发计划、国家自然科学基金等项目资助下,研究团队首先对5月龄的HD-KI猪及野生型猪纹状体进行单核RNA测序,并与HD患者及两种小鼠模型的公开数据进行跨物种整合,绘制了首张高分辨率纹状体细胞图谱。
这张图谱揭示了一个关键差异:仅在HD患者和HD-KI猪的纹状体中,存在细胞毒性CD8+ T细胞的显著浸润,且伴随T细胞受体的克隆扩增,而这一现象在小鼠模型中完全缺失。
这一发现首次将T细胞介导的适应性免疫与HD的病理进程在大型哺乳动物模型中联系起来。那么,这些T细胞是如何被招募到纹状体的?它们又与神经元死亡有何直接关系?
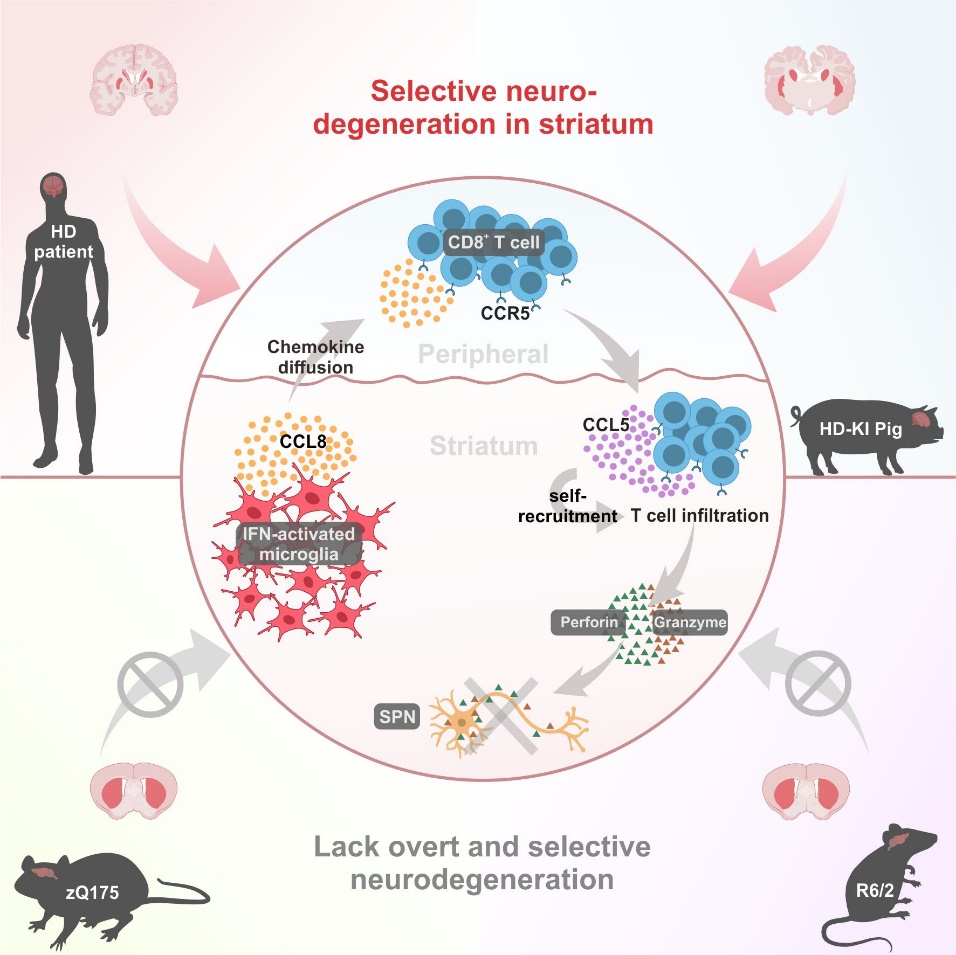
物种特异性小胶质细胞招募CD8+ T细胞加剧亨廷顿病神经退行性病变的示意图。
为了回答这些问题,团队利用细胞通讯分析,结合空间转录组学技术,清晰地勾勒出这场发生在脑内的“致命对话”的完整路径:
第一步:“哨兵”警报。 在HD纹状体中,研究团队鉴定出一群独特的“干扰素响应性”小胶质细胞亚群。这些小胶质细胞作为大脑的常驻免疫细胞,在感知到病理刺激后,被显著激活并大量扩增。它们的一项重要功能是大量分泌一种名为趋化因子配体8(CCL8)的信号分子。
第二步:“杀手”招募。 分泌的CCL8在脑组织中形成趋化梯度,作为一种“邀请函”,特异性招募那些表面高表达其受体CCR5的免疫细胞。而被招募的,正是携带杀伤武器的CD8+细胞毒性T细胞。这些T细胞在CCL8的指引下,穿越血脑屏障,浸润至纹状体实质,并在局部发生克隆扩增。
第三步:“处决”神经元。 抵达战场后,被激活的CD8+细胞毒性T细胞释放其经典的杀伤武器——穿孔素和颗粒酶。穿孔素在神经元细胞膜上打孔,颗粒酶则通过这些孔道进入神经元内部,启动细胞凋亡程序,直接攻击并诱导邻近的纹状体神经元走向死亡。
至此,一条从固有免疫(小胶质细胞)启动,到适应性免疫(CD8+ T细胞)执行的完整免疫病理通路被清晰地揭示出来。论文共同第一作者、暨南大学博士研究生林颖琪介绍,为验证这一机制的普适性,团队在HD小鼠模型中进行了“功能获得”实验。
为长期争议提供机制解答
在原本不表达CCL8、也无T细胞浸润的HD小鼠纹状体内注射CCL8,成功诱导了CD8+ T细胞的浸润和神经元损伤,复刻了HD-KI猪模型的关键病理。反之,通过中和抗体阻断CCL8的活性,则显著减少了T细胞的募集,并有效缓解了神经元损伤。这一正反验证,如同给研究结果加上了一把坚固的锁,将CCL8确立为该免疫病理通路中的关键节点,也使其成为一个极具潜力的治疗靶点,为未来的治疗提供了新的希望。
记者了解到,该研究首次报道了CCL8介导的CD8+ T细胞向HD脑内迁移的现象。尽管这一免疫机制在其他神经退行性疾病中已有报道,但T细胞介导的适应性免疫在HD中的作用此前一直是领域内悬而未决的争议问题。
既往研究虽提示HD中存在T细胞相关标志物的上调,但该研究首次将这一现象明确地与CD8+ T细胞群联系起来。正如审稿人所言:“这是一项设计精妙的研究,为领域内长期未解的重要问题提供了令人信服的机制性解答。”
闫森指出,该研究的核心创新体现在三个方面:一是模型创新,利用大动物模型突破了小鼠模型的局限;二是发现创新,全球首次证实T细胞脑内浸润是HD的病理事件之一;三是靶点创新,提出并验证了靶向CCL8-CCR5信号轴的全新免疫治疗策略。
“我们成功揭示了一条从固有免疫(小胶质细胞)启动,到适应性免疫(CD8+ T细胞)执行的完整免疫病理通路,不仅有力回应了领域内关于适应性免疫是否参与HD病理的长期争议,也为未来开发神经免疫调节疗法奠定了坚实的科学基础。”闫森说。
相关论文信息:https://doi.org/10.1038/s41551-026-01621-x
| 分享1 |
| 相关资讯 |
| 图片资讯 | 更多 |




| 一周资讯排行 | 更多 |
关于我们 | 网站声明 | 服务条款 | 联系方式
京ICP备 14047472号-1
 京公网安备 11010502030844号
京公网安备 11010502030844号

